我国科学家开发基因写入新工具中国科学院动物研究所
4月30日,中国科学院动物研究所李伟与王皓毅团队合作在《自然-生物医学工程》(Nature Biomedical Engineering)发表题为Non-viral targeted integration of large DNA in primary human T cells independent of double-stranded DNA breaks的研究论文,报道了一种名为 PRIME-In 的新型基因编辑平台。该平台无需引发基因组 DNA 双链断裂,即可将大片段外源 DNA 高效、精准地整合到人类原代 T 细胞的基因组中,为安全、高效的非病毒 CAR-T 细胞制备提供了全新解决方案。中国科学院动物研究所研究生方森、助理研究员唐娜、研究生李伊芸和郭书宇、博士后陈阳灿为该文章共同第一作者,李伟研究员、王晨鑫副研究员和王皓毅研究员为共同通讯作者。
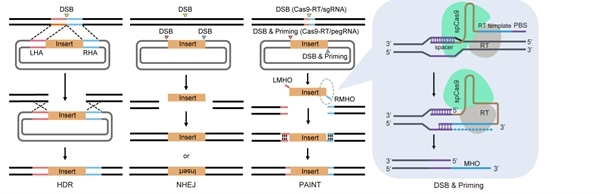
在基因组中实现大片段基因的靶向精准写入是基因和细胞治疗等领域的重大需求,但目前在技术上仍存在多种挑战。李伟团队2023年首次在Cell Discovery发表PAINT(Primed micro-homologues-assisted integration)系统,其核心原理是利用先导编辑器在供体质粒上生成3′单链微同源臂,再通过基因组双链断裂触发供体质粒上的外源基因在基因组上的整合。该机制被命名为PMEJ(Primed micro-homology-mediated end joining),它摆脱了传统同源重组修复中速率限制性的长距离DNA末端切除步骤。借助PAINT方法,团队在多种细胞中实现了远超传统HDR策略的靶向整合效率,将长度为2.5kb 的转基因以高达80%的整合效率插入基因组,并在原代 T 细胞中成功制备了具有特异性肿瘤杀伤能力的功能性CAR-T细胞,充分验证了单链微同源臂策略的巨大潜力。
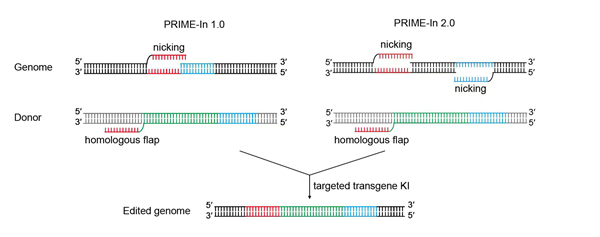
PRIME-In是基于团队此前开发的PAINT技术的进一步重大升级。PRIME-In平台巧妙绕开了双链断裂。它利用先导编辑器在质粒供体上生成一段称为“微同源臂”的单链突起,同时仅让基因组上产生一个小切口,两者配对后引导细胞内源DNA聚合酶完成长片段合成与整合。整个过程无DNA双链断裂修复途径的参与,从源头上规避了由此带来的基因毒性。
经过编辑器设计、供体优化和递送组分的系统提升,PRIME-In在细胞系中实现了最高85%的定点整合效率,并能处理长达10 kb的大片段。针对原代T细胞,团队通过引入密码子优化的分裂型先导编辑器mRNA、抑制机体DNA感知的病毒蛋白 UL36/UL37x1以及先天免疫抑制剂A151等,显著降低了质粒毒性,使报告基因的敲入效率达到约60%,CAR的整合效率达到约50%,并在7天内获得相当于起始数量11倍的工程化T细胞。
高通量测序显示,PRIME-In在原代T细胞编辑中的基因组整合精确度超过99%,几乎不引发染色体易位和脱靶整合,编辑副产物远低于传统的HMEJ等方法。双链断裂的避免也使得p53介导的凋亡通路不被过度激活,T细胞的活力和扩增能力因此得到更好保留。在体内实验中,PRIME-In构建的 CD19 CAR-T细胞能够有效清除小鼠体内的Raji肿瘤,其中靶向AAVS1 位点的CAR-T细胞在长期肿瘤控制和功能持续方面表现尤为突出,疗效与慢病毒转导的CAR-T细胞相当。此外,该方法还展示了在人胚干细胞等多类型细胞中的应用潜力。
PRIME-In介导的基因写入高效精准,规避了现有的非病毒定点整合方法必须切断基因组双链所引发的染色体易位、大片段缺失及细胞凋亡等问题,为CAR-T细胞疗法等基因编辑细胞药物的生产提供了更安全、更高效的策略。
PAINT系统工作模式图
PRIME-In系统工作模式图