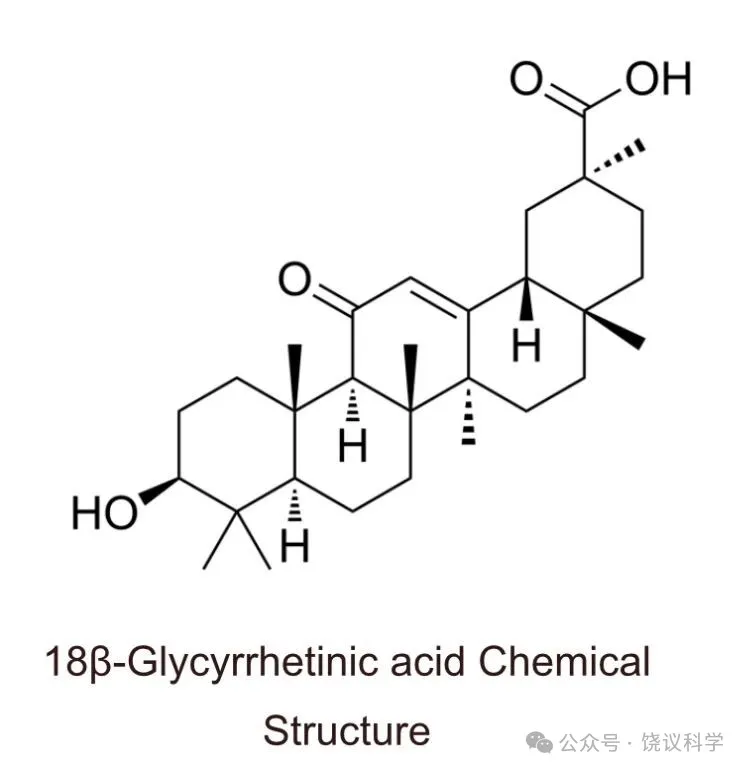
中药化学分子研究:甘草次酸与Warburg效应机器翻译
中药的科学研究,是中药发展的必由之路。
但研究中药却不是我实验室的必然工作。我们实际上没有计划做中药的研究。
我做过屠呦呦和青蒿素的科学史,但那是与北大医学部人物学部的张大庆和他的研究生黎润红的合作,与我的实验室无关。
我在北大的实验室,突然研究中药的单体化学分子,完全是误打误撞。我是安排的实验室多个研究生(北大都是直博生,我和一公回国后,北大清华的生命科学已经多年没有硕士生了)筛选一些分子及其作用。朱晨用的一个小分子库,是从国外购买的,发现有作用的分子里面,居然有一个是中药甘草来源的单体化合物甘草次酸(18β-GA)。朱晨观察到某种作用后,因为她还有其他重要观察,所以我请她专注那个课题,她有重要发现(且听明年分解)。我请夏冰心接朱晨的初步发现,研究18β-GA的机理。
18β-GA有抗癌作用,是其他多个研究课题组已经发现并报道的。但它的作用需要什么,并不清楚。
夏冰心用体外培养细胞系可以观察到18β-GA的杀癌细胞作用。这是验证其他人的发现。我安排她去北大魏文胜实验室学习分子生物学筛选方法(CRISPRi),用CRISPR的方法筛选可以抑制18β-GA作用的基因。她学的很快(也说明魏老师实验室的技术特别好,魏老师及其实验室的同事热心教我们)。很快掌握了技术,而且探索不同的检测可能。第一个检测拿不到很可靠的结果,换了第二个方法:看细胞死还是不死。魏老师也说过,用死亡来筛选最有效,我们验证了魏老师的建议。
用18β-GA孵育癌细胞,可以杀死癌细胞。而如果用CRISPRi方法筛选很多sgRNA的时候,有些sgRNA可以阻止18β-GA杀癌细胞的作用。我们把这些sgRNA拿出来,基因测序,然后多次同样筛选,几次都能富集的sgRNA就可能是对于18β-GA杀癌细胞所必需的基因。
我们拿到了多个基因,而且多个可以被反复验证。
在这些基因里面,有两个很有趣:它们有相关性。一个基因编码转运乳酸的蛋白质(学名:乳酸转运体,MCT1)。一个基因编码的蛋白质辅助MCT1。那么这就有趣了。
这时,我们学习文献。
在癌症领域,有一个著名的Warburg效应。这是1923年德国科学家、诺奖得主Otto Warburg发现的。通常,细胞在氧气充足的情况下,进行氧化磷酸化,缺氧的情况下进行糖酵解。Warburg发现,癌细胞氧化磷酸化减少,糖酵解增加。这一效应很快被另外一对诺奖得主所重复,Getty Cori和Carl Cori夫妇马上将这一效应命名为Warburg效应。
后来的研究证明,癌细胞在有氧的情况下,增加了糖酵解,但没有减少氧化磷酸化。所以,Warburg效应的正确表述是:癌细胞在有氧情况下增加糖酵解。
糖酵解是所有学习生物化学的学生都被要求死记硬背的一条通路。我实验室每一个学生都曾经被折磨过。一般难以记住其中的细节,容易记住所谓产生了多少个ATP。但糖酵解很简单的一个结果是:乳酸增加。因为乳酸是糖酵解的必然产物。
癌细胞的糖酵解增加,导致乳酸增加。如果乳酸太多,癌细胞就会被自己酸死。所以,很多癌细胞就通过增加MCT1的表达,把乳酸转运出去。
这就有趣了,癌细胞增加糖酵解,糖酵解增加乳酸,如果癌细胞要避免自杀,就要增加MCT1。
文献读到这里,就太有趣了。我们的发现,意味着甘草次酸可以通过MCT1而进入癌细胞,从而杀死癌细胞。
有了这一假设,夏冰心就做了一系列实验,证明甘草次酸确实是通过MCT1而转运进入癌细胞,从而杀死癌细胞。
这一研究非常有趣,对研究生是很好的科学和技术训练。有偶然,有文献学习,有思考,有技术,有严格的实验。
筛选带来的是惊讶,而不是事先知道结果。实际上,事先只设计了一步实验,后面的实验是根据前面的实验结果而一步一步设计。
像是一个侦探故事。
研究生是侦探,人类对自然的侦探。
这一研究也可以有意义,意义的大小需要时间检验。
一个可能比较大的意义是:甘草次酸的机理,等于是特异针对癌细胞,针对Warburg效应而杀细胞,那就是杀癌细胞。
这一机理提示可以用甘草次酸,或者它的衍生物,或者按这一机理设计其他抗癌药物,增加对癌细胞的特异性,减少副作用。
目前的缺点是:1)MCT1并非甘草次酸杀癌细胞的靶蛋白,只是让甘草次酸进入细胞,靶蛋白应该是其他;2)甘草次酸(18β-GA)本身的抗癌作用不是很强,所以用它不够。
但是,如果改变它的结构,增加抗癌作用,保留特异性,可能就很好。不改变它,而改变一个已知的强效抗癌药,但接上可以通过MCT1的基团,针对Warburg效应,也是一种方法。
还有一种可能,很毒的药物,因为缺乏特异性而副作用很大,但如果接上特定结构,有如甘草次酸的结构,从而专门进入MCT1,可能也可以特异针对癌细胞。
所以,一个研究不仅在于它本身有趣,还在于可以刺激更多的研究和设计】
靶向Warburg效应:乳酸转运蛋白MCT1及其分子伴侣在18β-甘草次酸杀伤癌细胞中的作用
夏冰心 朱晨 饶毅
Warburg效应癌症转运蛋白中草药
甘草是一种常用的中药,其主要成分是甘草酸,衍生产品18β-甘草次酸(18β-GA)具有抗肿瘤活性。本研究通过全基因组CRISPR筛选,确定了18β-GA敏感性所需的基因。我们发现乳酸转运蛋白MCT1及其膜分子伴侣BSG参与了18β-GA对癌细胞的杀伤作用。MCT1对于癌细胞摄取18β-GA是必要且充分的。BSG对于MCT1在细胞膜上的定位是必需的,因此对于18β-GA的摄取以及癌细胞的死亡至关重要。虽然已知癌症的Warburg效应会增加乳酸产生,进而选择更高表达MCT1的癌细胞,通过排出乳酸来增强癌细胞的存活,但我们的研究揭示了一个新的机会,即通过Warburg效应增加癌细胞对18β-GA的敏感性,从而杀死癌细胞。因此,我们的结果揭示了18β-GA敏感性的生物标志物,并暗示了利用Warburg效应使药物进入肿瘤细胞的可能性,这将激发对传统中药的进一步分子机制研究和改进。
1. 引言
在现代医学传入中国之前,传统中药已经为中国保驾护航数千年。其中最常用的中药之一是甘草(Glycyrrhiza glabra),它有着悠久的历史[1,2]。从其根部提取的主要化学物质是甘草酸,经肠道细菌水解后产生18β-甘草次酸(18β-GA)[3,4]。
癌症仍然是全球健康的重大挑战,传统治疗方法常常受到药物耐受性和不良反应的限制。癌症细胞代谢的一个标志是由Otto Warburg在一百年前发现的[5-7],并很快由Carl和Getty Coris证实[[8-12]。最初认为糖酵解增加而氧化磷酸化减少,但后来的共识是癌症细胞在有氧条件下仅增加糖酵解(“有氧糖酵解”),产生更多的乳酸[5-7,10,11]。
发现新型治疗剂和分子靶点对于推进癌症治疗至关重要。一些值得注意的抗癌药物是从植物中发现的,例如紫杉醇和长春碱,它们最终成为卵巢癌等常见癌症的一线治疗选择[13]。18β-GA已被发现具有抗癌效果[14,15],对多种癌细胞表现出广谱活性[16-19]。18β-GA可以抑制对癌症生长和转移至关重要的主要途径,例如PI3K/Akt、MAPK/ERK1/2和Akt/mTORC1/STAT3[14,17,20,21]。尽管对18β-GA的抗癌机制有很多研究,但关于允许18β-GA进入细胞的细胞膜分子基础知之甚少[22-24]。
CRISPR-Cas9提供了一种强大的基因修饰技术[25],衍生技术是应用CRISPR-Cas9进行基因功能筛选[26-30]。它可以用来寻找药物敏感性和耐药性的机制[29,31,32]。
在这项研究中,我们应用基于CRISPR-Cas9的筛选系统地寻找18β-GA反应所需的基因。我们发现单羧酸转运蛋白1(MCT1,也称为SLC16A1)及其膜分子伴侣basigin(BSG)是18β-GA敏感性所需的。
溶质载体(SLC)有助于细胞质和囊泡转运体。家族16(SLC16)在人类中有14个成员,它们是依赖于电化学Na+或H+梯度的次级主动转运体[33-36]。MCT1是SLC16家族的成员,是一种质子偶联的单羧酸转运蛋白,负责转运乳酸和丙酮酸等单羧酸[37-41]。BSG是MCTs的分子伴侣,对于MCT1、MCT3和MCT4在细胞膜上的定位至关重要[42-47]。在癌症中发现了MCT1的过表达[36,48-56]。MCT1允许乳酸从正在进行有氧糖酵解的癌症中运出,这对于癌症细胞代谢至关重要。先前针对癌症细胞Warburg效应的策略是通过化学化合物抑制MCT1[57-60]。由于乳酸很小,因此并不明显可以将有毒分子标记到通过MCT1的分子上。
我们的进一步研究表明,18β-GA依赖于MCT1被运输到癌细胞中,MCT1的高表达使细胞对18β-GA更敏感,从而表明像18β-GA这样比乳酸大得多的分子可以通过MCT1运输,因而可利用Warburg效应靶向癌细胞,为癌症治疗提供了新的策略。
2. 材料与方法
2.1 细胞培养试剂和抗体
H1975和A375细胞系由北京大学的魏文胜博士赠予。A375细胞在Dulbecco改良Eagle培养基(DMEM)中培养。H1975细胞在Roswell Park纪念研究所(RPMI)1640培养基中培养。所有细胞均补充10%胎牛血清(FBS),1%青霉素/链霉素,在37°C、5%CO2的湿润培养箱中培养。
DMEM、RPMI 1640、胰蛋白酶和FBS购自Life Technologies/Gibco Laboratories(纽约州格兰德岛,美国)。Lipofectamine 3000(Invitrogen)。18β-GA和AZD3965购自MedChemExpress(MCE)(中国上海),溶于DMSO。
2.2 细胞活性测定
将细胞以104个/孔的密度接种在96孔板中过夜,然后用18β-GA在特定浓度下处理24或48小时(h)。处理后,使用CellTiter-Glo(Promega)、CCK-8(Abcam)和LDH细胞毒性检测试剂盒(Beyotime)测量每种浓度的细胞死亡百分比,与DMSO处理的细胞相比。
2.3 慢病毒包装质粒文库和感染
对于慢病毒生产,转染前一天将HEK293T细胞在五个10厘米培养皿中以大约40%的密度铺板。在转染当天,将含有12 μg质粒DNA(4 μg质粒文库:4 μg psPAX2:4 μg pMD2.G)的混合物准备在500 μL预温的Opti-MEM培养基中。然后将该混合物与Lipofectamine 3000在额外的500 μL Opti-MEM培养基中混合。在室温下孵育30分钟后,将转染混合物逐滴加入HEK293T细胞中。转染后48小时收获病毒上清液,通过0.45 μm Acrodisc注射器过滤器过滤,分装,并在-80°C下储存以供后续使用。为了确定感染复数(MOI),将目标细胞以5×106个/孔的密度接种在六孔板中,并用不同体积的病毒上清液补充8 μg/ml聚布雷纳(Millipore,#TR-1003-G)在新鲜培养基中感染24小时。随后,将感染的细胞转移到15厘米培养皿中,并用2 μg/mL的嘌呤霉素进行选择。