为什么用去屑洗发水,头皮屑却越洗越多?中科院物理所
你一定有过这样的经历:被种草了一款去屑洗发水,刚开始用的半个月,头发顺滑、头皮清爽,仿佛打开了新世界的大门。但好景不长,用到第二瓶或者几个月后,头皮开始发痒,头皮屑不仅回来了,甚至比以前更多。
这时候,大多数人会觉得:“我的头发对这款洗发水产生耐受性了。”
真的是这样吗?
事实上,头发是死细胞,根本不会产生所谓的“耐药性” 。真正“搞鬼”的,是你头皮上的一场微观战争,以及洗发水里那些“过于尽职”的化学成分。
区分头发和头皮
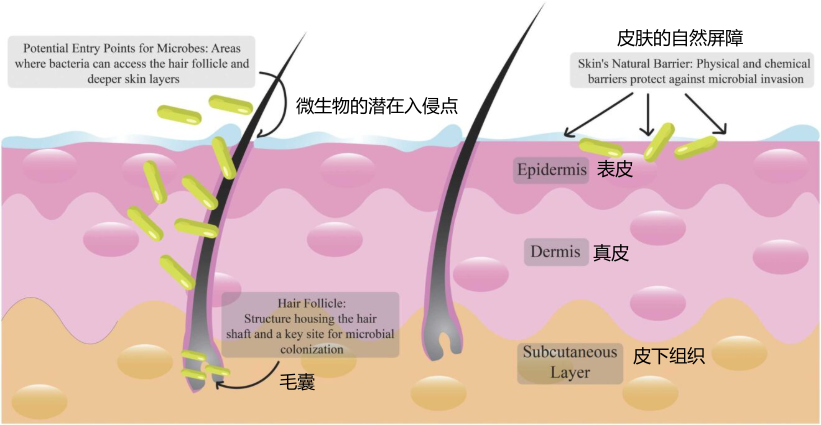
理解洗发水作用机制的首要前提,是区分发丝与头皮截然不同的生物学属性。发丝是完全角质化的死细胞结构,主要由角蛋白构成,不具备新陈代谢能力,没有神经末梢或血管分布。因此,发丝本身不可能产生生理学意义上的“耐受性”或“适应性”。它无法像细菌那样发生基因突变,也无法像人体细胞那样下调受体敏感性。
相反,头皮是活性皮肤组织,拥有丰富的皮脂腺、汗腺、免疫细胞以及复杂的微生态系统。头皮的皮脂分泌率远高于面部和身体其他部位,为微生物提供了丰富的脂质营养来源。头皮对化学刺激(如表面活性剂、防腐剂)会产生免疫应答,且其表面的微生物群落会随环境变化(pH值、油脂成分、抗真菌剂浓度)发生动态演替。因此,所谓的“洗发水失效”,实则是头皮微环境与微生物群落对长期单一化学干预做出的适应性调整。
到底是谁建立起了耐受
在药理学中,快速耐受指的是药物在重复给药后,机体反应性迅速降低的现象。虽然这一术语常被用于描述药物疗效的减退,但在洗发水的使用场景中,真正发生“耐受”的主体并非宿主(人),而是定植于头皮的病原微生物——马拉色菌。
这种适应性并非传统意义上的抗生素耐药性(尽管基因突变确实存在),更多表现为表型适应。例如,长期暴露于亚致死浓度的抗真菌剂中,马拉色菌会通过形成生物膜(Biofilm)来构建物理屏障,阻碍活性成分的渗透。这种由单一种类洗发水长期使用导致的微生态平衡漂移,使得原本被抑制的菌群在生物膜的保护下重新繁衍,导致头皮屑症状复发,给我们造成了“产品失效”的错觉。
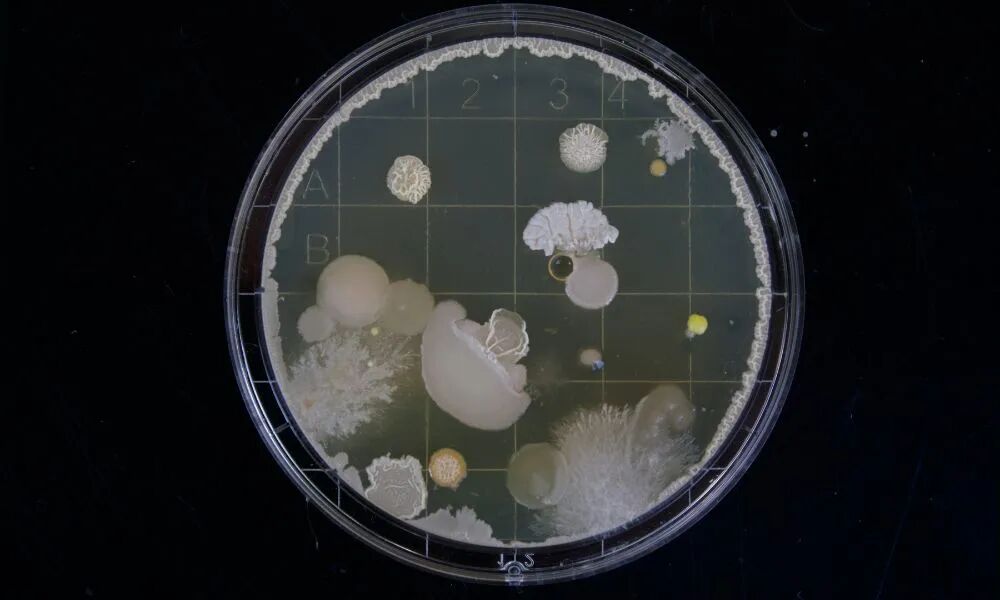
头皮屑是如何形成的
马拉色菌(主要是限制马拉色菌 M. restricta 和球形马拉色菌 M. globosa)是人类皮肤表面的常驻共生菌。与其真菌近亲不同,马拉色菌的基因组中缺失了编码脂肪酸合酶(Fatty Acid Synthase)的关键基因,这使其成为一种脂质依赖性微生物。它们无法自身合成长链脂肪酸,必须依靠分泌多种脂肪酶和磷脂酶,将头皮皮脂腺分泌的甘油三酯水解为甘油和游离脂肪酸。
这一代谢过程是头皮屑产生的生化源头。马拉色菌选择性地摄取特定的饱和脂肪酸(如棕榈酸)用于构建自身的细胞膜,而将代谢副产物——不饱和脂肪酸(特别是油酸)以此类推遗留在头皮表面。油酸具有极强的渗透性,能够穿透角质层细胞间隙,破坏皮肤屏障功能。对于敏感个体,渗透进入表皮深层的油酸会触发角质形成细胞释放炎症介质,导致表皮细胞增殖速度异常加快,未完全成熟的角质细胞成片脱落,形成肉眼可见的头皮屑。
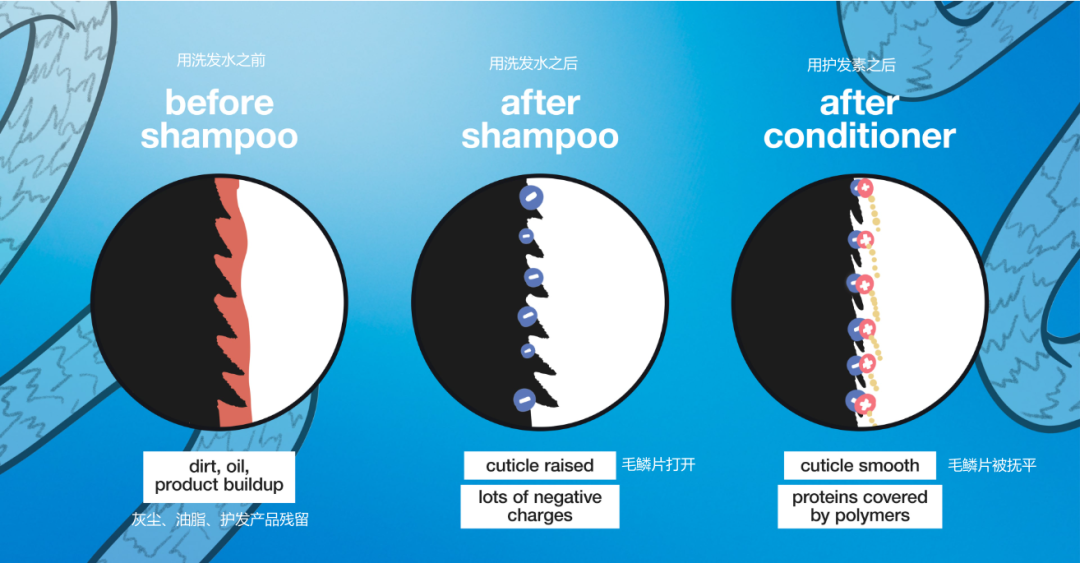
去屑洗发水是如何起作用的
市面上的去屑洗发水主要通过添加抗真菌活性成分来抑制马拉色菌的生长。不同的成分有不同的作用靶点,这也解释了为何长期依赖单一成分可能导致防线失效。
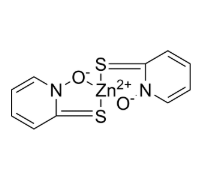
吡啶硫酮锌(Zinc Pyrithione, ZPT): ZPT 曾是应用最广泛的去屑剂。其作用机制独特,主要是作为铜离子载体,促进环境中的铜离子大量流入真菌细胞内,导致细胞内铜浓度达到毒性水平,从而破坏含铁-硫簇蛋白的功能,抑制真菌代谢。然而,这种机制依赖于微环境中的金属离子平衡。
酮康唑(Ketoconazole): 属于咪唑类抗真菌药,主要通过抑制细胞色素 P450 酶——羊毛甾醇 14α-去甲基化酶(cytochrome P450 enzyme, lanosterol 14α-demethylase)的活性,阻断真菌细胞膜重要成分麦角甾醇的生物合成,导致细胞膜通透性改变而死亡。
二硫化硒(Selenium Sulfide): 具有抗真菌和细胞抑制双重作用,既能抑制真菌增殖,又能减缓表皮细胞的更新速。
当长期使用同一种洗发水时,主要是在对微生物群落施加单一的选择压力。尽管马拉色菌不易像细菌那样迅速产生质粒介导的耐药性,但基因组学的研究表明,它们可以通过扩增 ERG11 基因拷贝数或上调药物外排泵(Efflux Pumps)来降低细胞内药物浓度,从而在持续的化学攻击下存活。