遭细菌污染,超300万瓶眼药水召回Yumi
据4月6日报道,美国联邦卫生部门近日发出警告,提醒消费者立即检查家中药箱。由于生产过程中存在无菌保障问题,超过300万瓶眼药水已在全美范围内被召回,涉及多个常见品牌和零售渠道。
新闻报道截图
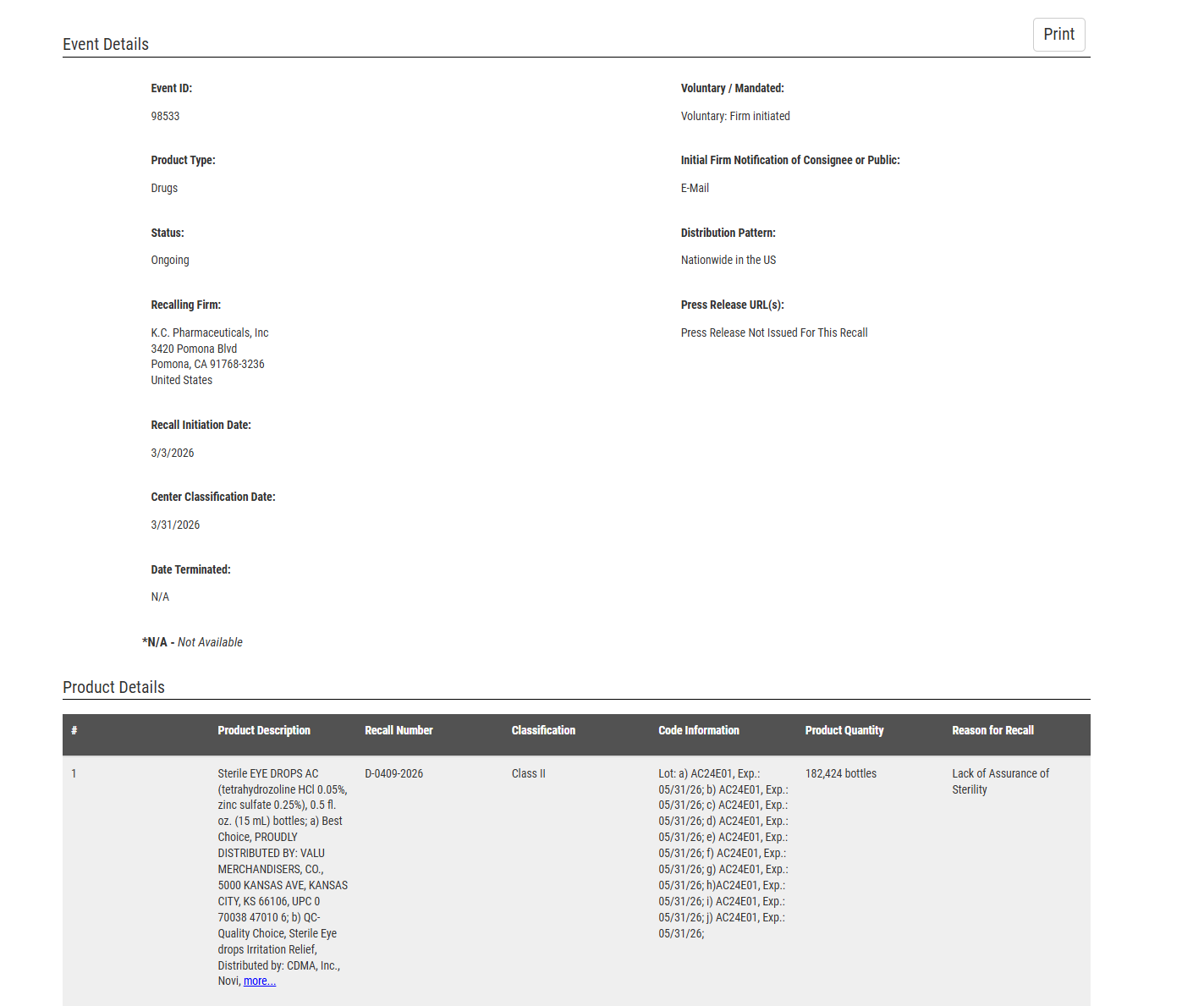
根据美国食品药品监督管理局(FDA)3月31日公布的信息,总部位于洛杉矶县波莫纳的K.C. Pharmaceuticals已主动召回约3,111,072瓶眼药水产品。
召回原因:无法确保无菌
此次召回的主要原因是“无法保证产品无菌(Lack of Assurance of Sterility)”。这意味着生产过程中可能未能完全防止细菌等微生物进入产品,从而存在感染风险。
被召回的产品种类较多,包括:
人工泪液(Artificial Tears)
高级缓解型眼药水(Advanced Relief)
去红血丝润滑眼药水(Redness Lubricant)
涉及多家知名零售商
相关产品通过多个大型连锁渠道销售,包括:
· 药店:CVS、Walgreens、Rite Aid;
· 超市:Kroger、H-E-B、Publix、Meijer、Harris Teeter;
· 其他渠道:Dollar General、Circle K;
· 批发及分销:Cardinal Health、McKesson,以及Leader、Equaline等品牌;
大部分受影响产品的有效期延续至2026年5月或10月。
目前尚无明确污染报告
FDA指出,目前并未明确证实这些产品已经受到污染,但生产过程未达到确保无菌的标准,因此出于安全考虑进行预防性召回。
此外,官方尚未公布具体的退款或更换方案。
消费者应立即停止使用
卫生部门建议,消费者一旦确认使用了相关批次产品,应立即停止使用。
如出现以下症状,应尽快就医:
消费者可通过以下方式进行核查:
1. 查看品牌
若产品来自以下品牌或渠道,应提高警惕:Walgreens、CVS、Rite Aid、Kroger、H-E-B等。
2. 查看批号(Lot Number)
重点检查以下开头的批次编号:AC、AR、LT、SU、RG、RL、SY、AT。
同时注意有效期为2026年的产品。
后续处理仍待明确
尽管FDA尚未公布具体退款流程,但业内预计,各大零售商可能会接受相关产品的退换申请。
目前,监管机构仍在持续跟进此事件,后续信息有待进一步公布。
FDA官网链接:https://www.accessdata.fda.gov/scripts/ires/?Event=98533