冷冻17年后睾丸移植回人体丁香园
2008 年,一名 10 岁男孩在接受化疗前,决定切掉一侧睾丸。
那块组织被切成小块,用慢速冷冻法降到液氮温度。冻存前,医生在显微镜下确认了精原细胞的存在。
17 年后,男孩长大成人,医生们把童年冻存的睾丸组织重新移植回他体内,并在一年时间内产生了成熟、有活动力的精子。
不久前,这个病例以预印本形式发表,记录了人类首例冷冻 17 年睾丸组织移植成功。而在这背后,还有数千名同样经历的患者,正在等待希望。
冷冻 17 年,人类首例
2026 年 3 月,比利时布鲁塞尔自由大学(VUB)和布鲁塞尔大学医院团队发布的一份 medRxiv 预印本(尚未经同行评审),报告了一项人类首例:
儿童期冻存的未成熟睾丸组织,经自体回植后在移植块内完成完整精子发生,产出成熟、有活动力的精子。
这名患者出生即被诊断为镰状细胞贫血,需要异基因造血干细胞移植才能根治,而移植前的预处理需要大剂量烷化剂化疗。
烷化剂是男性不育的高危药物,数据显示,大约三分之一接受过这类治疗的男性会在成年后出现无精子症。
2008 年,患者和家人做了一个不寻常的决定,在治疗前切除一侧睾丸用于冻存。
在当时,这还是一项实验性操作。2002 年,布鲁塞尔大学医院在全球率先开展未成熟睾丸组织冻存,但全球范围内没有任何人类回植成功的先例。
幸运的是,经过化疗,患者的镰状细胞贫血最终治愈。
2022 年,这名患者找到为他冷冻睾丸的研究团队,提出生育意愿。但接下来的两年多时间里,多次精液检查都显示「无精子症」;2024 年 12 月移植前评估时,对剩余的另一侧睾丸组织进行酶消化处理,全部细胞中也只检出 2 个形态异常的精子细胞。
自然受孕的可能性,基本归零。
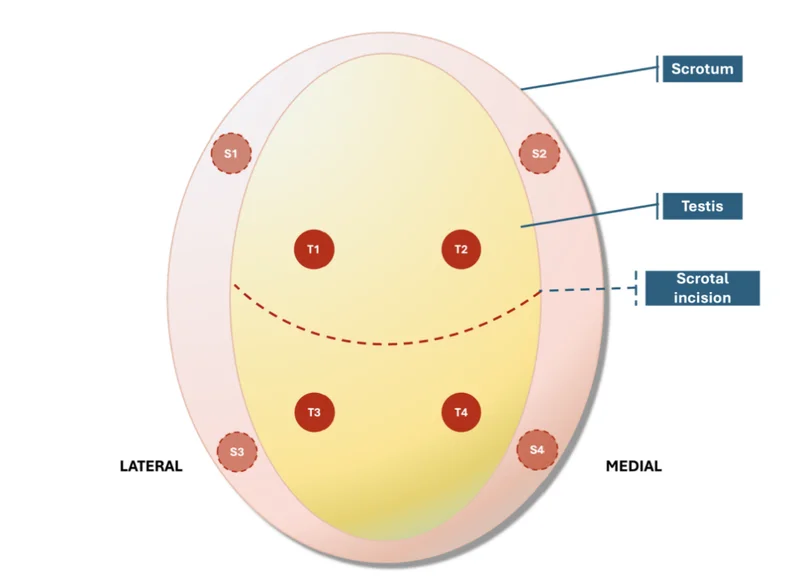
2025 年,这名患者正式接受了冷冻睾丸组织的移植手术。11 个解冻后的组织碎片(每块 4~21 mm³)被分为两组,4 块移植到睾丸内(标记 T1–T4),4 块移植到阴囊皮下(标记 S1–S4)。
移植部位示意。睾丸内位点 T1–T4,阴囊皮下位点 S1–S4。图源:参考资料 1
这台手术不只是为了恢复患者的生育能力,同时也是一次小型对照实验。研究团队想要回答一个具体问题,回植到原生睾丸环境内,是否真的优于回植到阴囊皮下?
一年后,所有移植组织被手术取回,并进行多维度评估。结果显示,睾丸内移植组的部分组织产生了成熟、有活动力的精子,而阴囊皮下组未达到这一水平。
研究还指出,患者冻存的组织本身精原干细胞数量「极低」,但即使如此微量的起始细胞,也足以触发完整的精子发生。这意味着未来不一定要冻存大量睾丸组织,少量样本也可能足够。
不过遗憾的是,由于移植区域没有连通输精管系统,患者的射精样本里目前依然没有精子。如果想要生育,需要进一步通过辅助生殖手段来实现。
也就是说,这例移植恢复了精子发生本身,但没有恢复自然生育能力。这两者之间还隔着一步辅助生殖。
冻存的睾丸,怎么活过来?
冻存本身就是一场为期数十年的赌注,没人能保证未来真的有技术能成功让这些组织复苏并成功回植。
事实上,围绕「如何让冻存睾丸组织重新产出可用精子」这个核心问题,目前在研究的技术路径不止一条。
路径一:组织块直接回植(也就是本次布鲁塞尔病例所采用的方案)。
这项技术的优势在于原生微环境最完整,对支持精子发生的间质细胞、屏障结构都有保留。但需要冻存一定数量的组织,回植需要开放手术。
目前,这条路径最关键的预临床里程碑发生在 2018 年。匹兹堡大学团队从 5 只青春期前的恒河猴身上取下睾丸组织冻存 5~7 个月,再解冻后移植回各自的背部和阴囊皮下。
8~12 个月后,研究团队取其中一只猴子的精子完成体外受精,将胚胎植入代孕母猴体内,顺利诞下一只健康雌性小猴。
上述诞生的小猴(图源:视频截图)
这是首例由冻存青春期前睾丸组织衍生而来的非人灵长类活产个体。在当时,研究团队就表示:「我们觉得这项技术已经准备好接受临床检验。」
但从猴到人这一步,此后数年里始终没有真正跨过去。
而本次布鲁塞尔的病例意味着,过去 20 多年里全球累积的 3000 多份冻存样本,第一次有了真实的临床应用依据。
路径二:精原干细胞悬液注射。
这条路径在冻存阶段就将睾丸组织进行酶消化处理,分离出精原干细胞悬液后保存;回植时再把细胞悬液注入患者的曲细精管系统,让这些干细胞在原来的位置上启动精子发生。
其优势在于,只需要少量细胞,对冻存样本量要求更低,同时创伤更小,整个操作不需要开放手术。
2023 年 11 月,匹兹堡大学 Kyle Orwig 团队完成了首例人类精原干细胞悬液注射。研究于 2025 年 3 月在 medRxiv 发布预印本,主要结论是注射安全可行,但精子发生是否真正恢复,仍待长期随访。
路径三:体外精子发生和睾丸类器官。
前两条路径都需要把组织或细胞放回人体内,而这条路径则完全跳过「回植」这一步,直接在体外培养系统中将精原干细胞诱导分化为成熟精子。理论上可以在体外彻底清除潜在的恶性细胞污染,避开自体回植的安全风险。
目前,有团队于 2011 年在小鼠原代睾丸组织块中实现了完整的体外精子发生,产物可以用于体外受精。但尚无人类和灵长类身上的突破。
而在人类睾丸类器官方面,也还没有任何团队能稳定产出可受精的成熟单倍体精子。
全球累计冻存睾丸样本超 3000 份
数据显示,全球每年新诊断的 0~14 岁男性儿童肿瘤约 14 万例,0~19 岁则超过 22 万例。其中相当一部分需要烷化剂化疗、全身放疗或造血干细胞移植。生存率提升的代价之一,是生育力受损。
而对青春期前的男性儿童来说,这件事更复杂。
成年男性在化疗、放疗等促性腺毒性治疗前,可以通过精液冻存保留生育力,操作成熟、成本低、效果可预期。但青春期前的男孩睾丸里还没有成熟精子,只有处于静息状态的精原干细胞。
也因此,冻存睾丸组织或睾丸细胞成了唯一可行的方案。
自 2002 年布鲁塞尔大学医院启动全球首个未成熟睾丸组织冻存项目以来,欧洲多个国家、美国、加拿大、以色列、澳大利亚都已建立类似的临床冻存项目,覆盖网络仍在扩大。
截至 2025 年,全球累计冻存睾丸样本超过 3000 份。
回到开头的病例,按照试验设计,目前所有移植组织已在术后一年被手术取出,从取出组织中获得的这批精子会被冷冻保存,留待后续辅助生殖使用。
研究团队表示,将持续随访这名患者后续的胚胎发育、妊娠进程,以及一旦后代诞生,长期的健康指标。