新研究揭示Dicer酶“双口袋机制”中国科学报
人类生命信息以DNA编码储存,通过信使核糖核酸(RNA)传递并执行。在RNA的世界里,Dicer酶扮演着“精密剪刀”的关键角色——它将双链RNA切割成短小片段,使其进入RNA干扰通路,通过碱基互补配对识别并沉默错误或不需要的基因信息。自20世纪90年代末RNA干扰机制被发现以来,Dicer酶作为这一过程的核心酶,始终是分子生物学领域的研究热点。
近日,香港科技大学副教授阮俊英团队在《自然》发表最新成果,成功揭示了人类Dicer酶精准调控微小RNA的分子机制。该研究修正了延续20余年的经典认知,为基因调控研究、疾病机制解析及新一代RNA疗法开发奠定了关键基础。
发现新口袋,颠覆旧认知
微小RNA是一类长度约为22个核苷酸的非编码RNA,在细胞分化、增殖、凋亡及免疫应答等关键生理过程中发挥精细调控作用。其生成异常与多种癌症、免疫系统疾病及遗传病密切相关。因此,揭示Dicer酶如何精准切割微小RNA前体,对理解疾病分子根源具有重要意义。
Dicer酶作为RNA干扰(RNAi)通路中的关键核酸内切酶,是基因沉默技术的核心元件。过去20余年间,科学家普遍认为Dicer酶主要依赖一个偏好识别尿嘧啶(U)的5′端结合口袋实现切割,而对以鸟嘌呤(G)为首的RNA底物存在结构排斥。阮俊英团队的研究颠覆了这一传统认知。
阮俊英(右)领导,并由博士生Minh Khoa NGO(左)与Cong Truc LE共同完成。受访者供图,下同
“该研究最大的难点在于捕获Dicer酶与5′端不同核苷酸开头的RNA结合时的活性状态。”论文通讯作者阮俊英对《中国科学报》表示,此前研究要么仅获取了未结合RNA的Dicer酶非活性结构,要么仅观察到结合单一类型5′端RNA的酶活性状态,无法完整还原酶的真实作用过程。
据介绍,研究团队整合高通量生化实验与冷冻电子显微镜技术,通过结合不同RNA序列的Dicer酶进行冷冻电镜分析,成功观察到酶结构域(尤其是dsRBD和PAZ结构域)的运动过程,以及这些结构域如何像筷子一样重新排列,从而结合不同序列的RNA。
论文第一作者、香港科技大学博士生Minh Khoa Ngo指出:“冷冻电子显微镜技术让我们能够在原子分辨率上观察RNA底物与Dicer酶的结合过程。这些分子影像清晰地展现了该核酸酶针对不同RNA序列做出的动态调整,从根本上改变了我们对其功能的认知。”
团队采用了两步法。第一步是大规模并行切割实验,他们向Dicer酶投掷了数千种略有不同的RNA变体,观察其切割反应,产生了海量数据;第二步是冷冻电镜分析,将结合RNA的Dicer酶瞬间冷冻并在原子水平上成像,直观地看到RNA嵌入Dicer酶的“口袋”结构。
“通过高分辨率的分子影像,团队首次捕捉到Dicer酶在切割前发生的精细构象变化:Dicer酶先将RNA底物引导至正确切割位置,随后利用酶内结构域精准定位,最终进入‘切割就绪’形态。”Minh Khoa Ngo说。
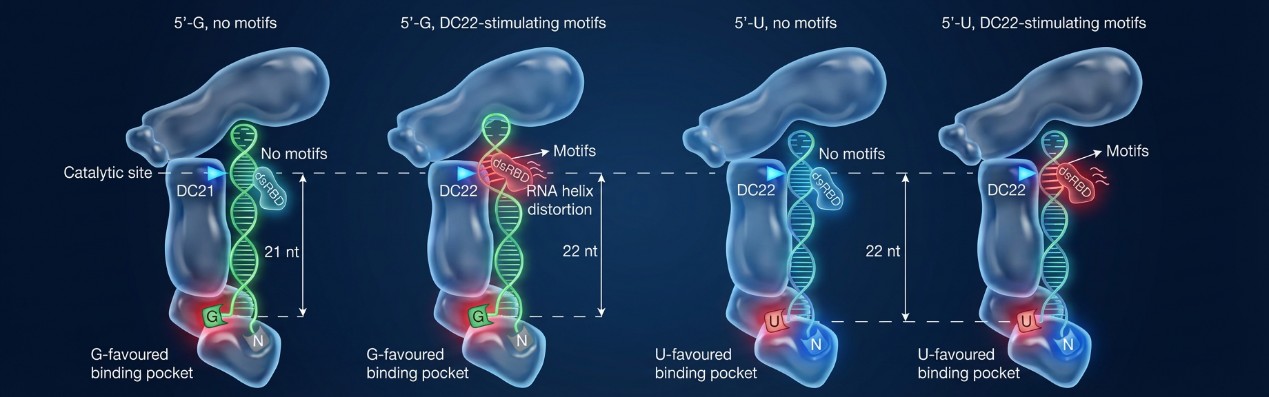
研究发现了两个关键的5′端结合口袋:一个是已知的偏好识别尿嘧啶的口袋,另一个是此前未知的、偏好识别鸟嘌呤的口袋。两个口袋共同构成“双口袋机制”,使Dicer酶能根据底物5′端核苷酸种类在两种口袋间动态选择,精准处理细胞内种类繁多的微小RNA前体和人工设计的RNA干扰触发分子。
双口袋,精准调控的关键
RNA切割的精准性至关重要。若Dicer酶切割位置错误,产生的RNA分子可能靶向错误基因或完全丧失功能。此前科学家仅知晓Dicer酶从RNA链末端开始测量长度,但尚不清楚它如何精准切割不同类型的RNA。
Dicer酶决策过程示意图。
该发现揭示了Dicer酶如何整合5′端核苷酸种类、RNA结构基序以及酶内部结构域的动态变化来共同维持切割精准度的分子机制,为理解微小RNA生物合成的多样性提供了统一的理论框架。
香港大学医学院助理教授Kwon Sung-Chul评价道:“阐明Dicer酶与多种底物结合的结构及作用机制,不仅填补了过去20年来分子生物学领域的一个研究空白,也为未来基于RNA干扰技术的疗法铺平了道路。”
从基础研究层面看,该发现重塑了人们对微小RNA生成过程的基本理解,为从分子根源解析癌症、免疫系统疾病及遗传疾病成因提供全新视角和潜在干预靶点。在应用转化方面,该成果最直接的价值体现在短发夹RNA(shRNA)技术优化上。
shRNA是人工合成RNA分子,经Dicer酶加工后形成小干扰RNA,可特异性沉默靶基因,广泛用于基础研究中的基因功能解析和基因治疗领域。但长期以来,科学家设计shRNA时,Dicer酶切割位置难以准确预测,有效shRNA筛选依赖反复实验,效率低且不确定性高。
如今,基于“双口袋机制”,研究团队可以有意识地设计具有特定起始核苷酸(鸟嘌呤G或尿嘧啶U)的短发夹RNA,使其精准靶向对应的Dicer酶结合口袋,从而确保RNA在预期位置被精确加工。这一策略有望显著提高shRNA的设计成功率与沉默效率,减少脱靶效应带来的安全隐患,为开发更有效、更安全的RNA干扰药物奠定坚实的分子基础。
该研究由阮俊英领导,Minh Khoa Ngo与Cong Truc Le等共同参与完成,不仅从原子层面解答了Dicer酶如何实现精准切割这一长期悬而未决的科学问题,更通过揭示“双口袋机制”,为下一代RNA疗法提供了可理性设计的结构蓝图。
下一步,研究团队计划探究当存在相互冲突的信号时——例如RNA以鸟嘌呤开头但其结构形状却要求不同切割位点的情况下——该机制如何协调工作。